Electrospray/ko
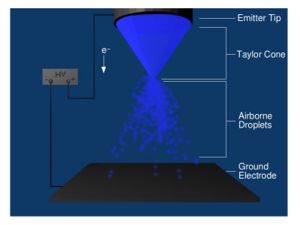
전기 분무 는 작은 모세관에 담긴 유체에 전기장을 가함으로써 발생하는 현상입니다. 구동하는 정전기력은 증발과 쿨롱 폭발의 단계를 순환하는 대전된 물방울의 방출을 유발하여 이상적으로는 기체 상태 이온 또는 매우 미세한 액체 에어로졸이 형성됩니다. 이 기술은 질량 분석 분야에서 널리 사용되었지만, W 산업용 페인팅, 입자 증착 및 유전자 치료와 같은 광범위한 다른 응용 분야에서도 작동하는 것으로 기록되었습니다. W
그러나 이러한 현대적 용도의 배열은 전기 분무의 기본 과학이 결코 새로운 것이 아니라는 사실을 숨깁니다. 사실, 전기 분무의 기원은 1882년에 출판된 Lord Rayleigh의 논문 "On the equilibrium of liquid conductor masses charges charge with electrical"까지 거슬러 올라갈 수 있습니다. [ 1 ] 그로부터 30년이 조금 넘은 후, John Zeleny는 전기 분무 현상을 목격한 최초의 사람이 되었고, 이후 "The electrical emission from liquid points, and a hydrostatic method of measured the electric intensity at their surface"에 자신의 관찰 결과를 발표했습니다. [ 1 ] 그 이후로 Taylor, Fenn, Dole 및 기타 여러 연구원의 지속적인 연구를 통해 전기 분무에 대한 과학의 이해와 응용 범위가 계속해서 발전해 왔습니다. [ 1 ] , [ 2 ]
작동 원리
문헌에서는 전기분무 이벤트를 일련의 3가지 고유한 단계로 구분합니다. [ 3 ]
- 시작과 방출
- 물방울 분열
- 가스상 이온 생성
아래에서는 이러한 각 단계를 개별적으로 논의하고 다양한 기계적 및 전기화학적 요소가 수행하는 지배적 역할을 설명합니다. 그림 1에서 장치의 개요를 찾을 수 있습니다.
시작 및 방출
정지 상태에서는 방출기 끝에서 용매의 증발을 구동할 만큼 충분히 강한 전기장이 없기 때문에 전기 분무 시스템에서는 활동이 관찰되지 않습니다. 방출이 시작되는 임계 전기장은 다음 관계로 특징지어집니다. [ 3 ]
어디:
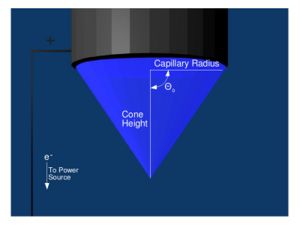
테일러 콘 W 형성을 통한 전기 분무 개시는 모세관에 수용된 액체에 전압 W를 인가함으로써 달성됩니다 (그림 1 참조). 필요한 전압의 크기 V onset 은 다음 관계에 따라 달라집니다. [ 1 ]
어디:
이 인가 전압을 변화시키면 방출기의 전기장 E ES 를 조작하여 결국 테일러 콘을 생성하는 수준까지 증가시킬 수 있습니다. E ES 는 다음 방정식을 통해 계산할 수 있습니다. [ 3 ]
어디:
대전된 공기 중의 물방울로 이루어진 그 결과 생성된 기둥은 전기장으로 인해 상대 전극을 향해 가속되고, 이후 일련의 물방울 분열 현상을 겪습니다.
물방울 분열
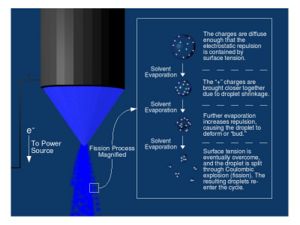
일단 공기 중에 떠 있으면, 액체 방울의 구조적 무결성은 용매화된 이온에서 발생하는 정전기적 반발과 표면 장력의 갈등에 따라 달라집니다. 레이리 한계라고 알려진 지점까지 표면 장력은 반발력을 견제하고 방울 파편화를 방지합니다. 그러나 증발로 인해 방울 크기가 지속적으로 줄어들면서 전하가 점차 더 가까워지고 반발력이 비례적으로 증가합니다. 결국 레이리 한계가 극복되고 방울은 쿨롱 폭발을 겪어 자손 방울로 분리되고 이 과정에서 프로세스가 재설정됩니다(그림 3 참조). 레이리 한계를 초과하고 핵분열이 발생하는 전하량 q R 은 다음과 같은 수학적 관계식으로 설명됩니다. [ 4 ]
어디:
그러나 이것은 단지 일반적인 지침일 뿐입니다. 많은 연구실에서는 레이리 방전(입자 분열이라고도 함)이 이 값의 70%~120%라고 보고했습니다. [ 4 ]
기체상 이온 생성
이온이 결국 기체 상태로 들어가는 방식을 설명하기 위해 두 가지 모델이 제시되었습니다. 이온 증발 모델(IEM)로 알려진 첫 번째 모델은 매우 작은(직경 수십 nm) 물방울에 존재하는 정전기적 반발이 실제로 이온을 표면에서 탈착시키기에 충분히 강하다고 가정합니다. [ 4 ] 반면, 전하 잔류 모델(CRM)은 증발과 쿨롱 폭발의 사이클이 최종적으로 기체 상태 이온이 생성될 때까지 계속된다고 간단히 설명합니다. [ 4 ] 어느 것이 더 우세한지는 아직 결정되지 않았으며, 실제로 두 모델이 서로 다른 상황(물방울 크기, 전하 밀도 등)에서 실행 가능한 모델이 될 수도 있고, 심지어 섞일 수도 있습니다. [ 3 ]
IEM에서 용매 표면으로부터 이온 증발의 가능성은 Gibbs 자유 에너지 W 의 관련 변화를 조사하여 결정할 수 있습니다 . 전체 값이 음수이고 활성화 에너지 W 장벽이 극복되면 반응이 자발적으로 발생할 수 있습니다. Iribarne과 Thomson의 모델과 Born의 모델은 모두 이 사건을 수학적으로 설명하려고 하지만 전자는 여러 요소를 고려하지 못하고 후자는 실험적으로 자유 에너지를 심각하게 과소평가하는 것으로 나타났습니다. [ 3 ]
그러나 핵분열과 용매 증발로 인한 점진적인 파편화가 기체 상태 이온의 생성으로 이어진다는 CRM의 견해에는 고유한 어려움이 있습니다. 일단 물방울이 불과 수 nm 크기에 도달하면 (가정된) 동일한 전하 분포가 손실되고 켈빈 방정식 W 로 인해 증기압 W가 이동하기 때문에 레이리 방정식이 무너집니다 . [ 3 ] 대신 나머지 이온은 용매 분자 돌출부에 갇히고 용매가 아닌 이온이 결국 IEM을 통해 증발한다고 생각됩니다. [ 4 ]
전기분무를 현실로 만들다
전기분무 장치를 구성하는 데 사용되는 중앙 설계와 구성 요소는 본질적으로 동일하지만, 응용 분야에 따라 종종 사용자 정의가 필요합니다. 아래에서 기본 직류 W ES 장치를 구성하는 프로세스를 설명하고, 다양한 용도에 필요할 수 있는 수정 사항을 자세히 설명합니다.
재료 및 도구 요구 사항
전기분무 장치를 설치하기 위한 절대적인 기본 요구 사항은 다음과 같습니다.
- 최소 1kV의 전위차를 생성할 수 있는 전원 공급 장치 W (대부분의 경우 전류 출력은 2차적인 관심사). 필요한 정확한 값은 응용 프로그램에 따라 크게 다릅니다. 고전압 증배기 W가 더 저렴한 대안으로 사용될 수 있지만, 이는 아직 입증되지 않았습니다.
- 일반적으로 직경이 0.1mm 이하인 강철 모세관인 방출기(기억하세요, 직경이 작을수록 분무를 생성하는 데 필요한 전압이 낮아집니다). 일부 그룹에서는 고유한 장점과 단점을 도입하는 실리카 기반 모세관 [ 5 ] 을 사용하기 시작 했고, 다른 그룹에서는 방출기 내부에 실리카 모노리스를 사용하여 새로운 효과를 생성했습니다. [ 6 ]
- 에미터와 반대쪽에 놓일 접지(전기) W 전극. 이것은 지구와 접촉하는 금속판만큼 간단할 수 있습니다.
- 원하는 용도에 필요한 화학물질/시약.
또한 일부 애플리케이션에는 다음과 같은 다른 구성 요소가 필요할 수 있습니다.
- 방출기에 용매를 공급하기 위한 정밀 제어가 가능한 용매 펌프입니다.
- 고전압 출력 변압기, RF 증폭기 및 파형 발생기( 교류 전류 W를 사용하는 경우 기존의 직류 전류 사용과 대조되는 새로운 방법). [ 7 ] , [ 8 ]
- 코로나 방전 W를 방지하기 위해 질소를 공급하는 네뷸라이저 W가 있는 폐쇄된 챔버가 필요할 수 있습니다 .
- 전압계 W , 전류계 W , 망원경 장비, 카메라 등의 특성화 장비 .
도구와 관련하여 여기에 설명된 기본 설계에는 특별한 것이 필요하지 않습니다. 어떤 경우에는 탐색 중인 프로젝트 유형에 따라 미세피펫 풀러와 같은 보다 특수화된 장치가 필요할 수 있습니다. [ 5 ] , [ 9 ]
건설
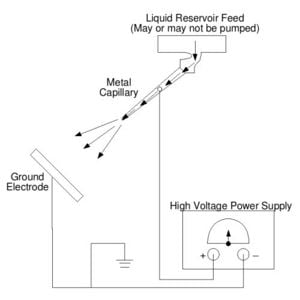
전기분무 시스템의 실제 조립은 간단하고, 계획은 비교적 간단합니다(그림 4 참조). 응용 프로그램에 따라 몇 가지 사항이 다를 수 있습니다. 몇 가지 예는 다음과 같습니다.
- 용매 방출기를 보완하기 위해 정밀하게 조절 가능한 용매 펌프와 함께 용매 저장조를 사용해야 할 수도 있습니다.
- 방출기 끝에서 타겟/접지까지의 거리는 적용 유형에 따라 달라집니다(예: 질량 분석의 경우 몇 mm에 불과하지만, 유전자 치료의 경우 일반적으로 2cm에 가깝습니다).
- 폐쇄된 챔버 환경과 질소 분무기가 필요합니다.
실제로 문헌 자체에서는 전기분무 장비를 최적으로 조립하고 제대로 작동하는지 확인하는 방법에 대한 세부 사항이 모호하므로, 이 분야에 대한 개인적인 경험이 있는 분이 계시다면 큰 도움이 될 것입니다.
작업
장치가 올바르게 조립되면 일반적으로 작동을 시작하는 데 필요한 단계는 다음과 같습니다.
- 용매를 방출기/저장소에 넣습니다.
- 대상 자료가 올바르게 설정되었는지 확인하세요.
- 1과 2를 다시 한번 확인하고, 계측기가 잠재적으로 전도성이 있는 물질로부터 절연되어 있는지 확인하세요.
- 전원을 활성화합니다.
전기 분무가 시작된 후, 완료될 때까지 반응을 모니터링할 수 있으며, 완료 시 전원을 비활성화해야 합니다. 시술 중에 도달한 전압은 치명적일 수 있거나 심각한 신체적 상해를 입힐 수 있으므로, 시술 중에는 기기와 가까이 있거나 접촉하지 않는 것이 매우 중요합니다.
장치를 유지 관리할 때는 변형을 방지하기 위해 방출기 팁을 물리적 스트레스로부터 깨끗하게 유지하는 데 특별한 주의를 기울여야 합니다. 또한 모든 구성 요소는 금속 표면의 부식을 최소화하기 위해 습기가 없는 환경에 보관해야 합니다.
전기분무를 이용한 작업 및 혁신
전기분무는 다양한 산업과 연구 도구로 응용되는 강력하고 적응력 있는 도구입니다. 다음은 전기분무가 사용된 몇 가지 영역입니다.
- 질량 분석법 [ 2 ] , [ 9 ] , [ 10 ] - 앞서 언급했듯이 전기 분무는 샘플 크기를 줄여 분석물의 분해능을 개선하는 데 도움이 되는 질량 분석법에 사용되었습니다. 여전히 논란이 있지만 역학은 비교적 잘 특성화되었지만, 이 분야에서 혁신하기는 어렵습니다. 왜냐하면 질량 분석기가 필요하기 때문이며, 이는 일반적으로 상업적으로 판매되며 특수하게 적합한 전기 분무 장치에 이미 결합되어 있기 때문입니다.
- 나노입자 의 제조 [ 1 ] - 전기 분무의 증발 및 핵분열 단계 동안 달성된 작은 부피는 제어된 반응 용기로 활용되어 알려진 크기의 무기 나노입자를 제조할 수 있었습니다. 이는 크기가 감지되는 방출 파장에 영향을 미치는 양자점 W 영역에서 특히 중요합니다 . 그러나 이를 제외하고 나노 제조에서 전기 분무를 사용하는 것은 여전히 많은 잠재력을 지닌 비교적 새롭고 손길이 닿지 않은 분야로 남아 있습니다.
- 마이크로어레이 제작 W , [ 11 ] - 마이크로어레이는 생물학적 진단의 핵심 도구이며 알려지지 않은 물질을 특성화하고 잠재적으로 분리하기 위한 빠르고 다중화 가능한 방법을 나타냅니다. 전기분무를 활용하면 이 프로세스를 로봇화하여 도트 면역 결합 및 DNA 하이브리다이제이션 W 분석에 여전히 사용할 수 있는 방식으로 이러한 칩을 빠르게 생산할 수 있으며 주어진 표면 단위에 대해 사용 가능한 정보 밀도를 높일 수 있다고 가정되었습니다.
- 유전자 치료 [ 12 ] - 전기 분무에 대한 가장 새로운 응용 분야 중 하나는 생명 공학 및 유전자 공학 분야입니다. 일본의 연구자들은 전기 분무 장치를 사용하여 진핵 및 박테리아 세포에서 형질 전환 이벤트를 유발하는 데 성공하여 현재 기술과 비교할 때 세포 독성이 적고 재사용이 쉽고 휴대성이 뛰어난 방법을 보여주었습니다. 이 분야의 응용 분야는 여전히 매우 열려 있으며 다양한 환경에서 상용화 기회를 쉽게 제공할 수 있습니다.
- 제약 생산 [ 7 ] - 제약 개발의 핵심 영역 중 하나는 치료 물질을 분해되거나 다른 환자 조직에 영향을 미치지 않고 필요한 위치로 전달하는 것입니다. 이런 측면에서 마이크로캡슐화 W는 이 문제를 우회하는 가능한 방법을 제공합니다. 과학자들은 전기 분무를 사용하여 약물을 다른 물질의 "껍질" 내부에 격리하여 신체 내에서 새로운 특성을 부여할 수 있음을 보여주었습니다.
- 생분해성 섬유 스캐폴드 [ 7 ] - 전기 분무는 다양한 의료 시술에 사용될 수 있는 생분해성 미세 섬유를 합성하는 추정 방법으로 연루되었습니다. 초기 연구에서는 조직 공학용 스캐폴드 W 및 염증 반응 예방을 위한 생물의학 임플란트용 마스크와 같은 코팅으로서의 유용성을 보여주었습니다.
- 차세대 "랩온어칩 W " 시스템 [ 13 ] - 과학의 많은 측면이 계속해서 소형화됨에 따라 작은 공간에서 다양한 습식 반응을 빠르게 수행할 수 있는 "랩온어칩" 장치를 제작할 수 있는 잠재력이 계속해서 향상되고 있습니다. 이러한 분야에서 전기분무의 높은 적용성으로 인해 현재 연구에서는 미래의 칩 랩에 기능으로 통합할 수 있는 크기로 프로세스를 축소하려고 시도하고 있습니다.
- 박막 증착 W [ 14 ] - 아마도 전기 분무 응용 분야에서 가장 확장되는 분야 중 하나는 기판 표면에 박막을 증착하는 것입니다. 전기 분무 중에 방출되는 작고 대전된 입자는 코팅 효율성이 높은 것으로 밝혀졌으며 이론적으로 광범위한 산업 분야에서 사용되어 재료에 새로운 표면 특성을 부여할 수 있습니다.
전기분무와 지속 가능성
전기분무가 지속 가능한 개발 에 도움이 될 수 있는 두 가지 주요 분야는 다양한 역할을 수행할 수 있는새로운 나노입자 와 박막을 제작할 수 있는 잠재력에 있습니다 .
나노입자의 경우, 제조 목적으로 전기 분무 장치의 사용을 통합할 수 있는 많은 지속 가능한 응용 프로그램이 제안되었습니다. 이러한 것들의 샘플은 다음과 같습니다.
- 나노입자를 이용한 지하수 정화 .
- 2세대(대부분 박막 기술을 통해) 및 3세대 태양 전지 W를 개선합니다 .
- 입자 기능화 소재(예: 의류 에 항균 효과를 주기 위한 은 나노입자)
박막의 경우 지속 가능성 목표 달성을 촉진하는 데 도움이 되는 다른 옵션도 많이 있습니다.
- 자체 세척 표면.
- 탄소 격리 박막.
- 앞서 언급한 대로 2세대 태양 전지에서는.
또한 전기 분무를 통한 유전 공학 분야의 새로운 발전으로 우수한 성능을 보이는 작물/가축 품종의 보다 빠른 개발이 가능해질 수 있다는 점도 주목할 만합니다. 이를 통해 농업 운영에 필요한 토지의 양이 줄어들고, 더 혹독한 기후에서도 농업이 번성할 수 있으며(식품 운송 비용 감소), 더 위험한 해충 관리(예: 살충제 및 제초제)의 필요성이 사라질 수 있습니다.
참고문헌
- ↑다음으로 이동:1.0 1.1 1.2 1.3 1.4 살라타 OV. 2005. 나노기술 도구: 전기분무. Curr Nanosci 1(1):25-33.
- ↑다음으로 이동:2.0 2.1 Gaskell SJ. 1997. 전기분무: 원리와 실제. J Mass Spectrom 32:677-688.
- ↑다음으로 이동:3.0 3.1 3.2 3.3 3.4 3.5 Rohner TC, Lion N, Girault HH. 2004. 전기분무 이온화의 전기화학적 및 이론적 측면. Phys Chem Chem Phys 6:3056-3068.
- ↑다음으로 이동:4.0 4.1 4.2 4.3 4.4 Grimm RL. 2006. 전기장 유도 입자 이온화 질량 분석법과 전기 분무 질량 분석법의 메커니즘과 응용에 대한 기본 연구. 논문.
- ↑다음으로 이동:5.0 5.1 Barnidge DR, Nilsson S, Markides KE. 1999. 저유량 덮개 없는 전기분무 방출기 설계. Anal Chem 71:4115-4118.
- ↑ Wang P, Chen Z, Chang HC. 2006. 다공성 실리카 모노리스를 기반으로 한 통합 마이크로펌프 및 전기분무 방출기 시스템. 전기영동 27:3964-3970.
- ↑다음으로 이동:7.0 7.1 7.2 Yeo LY, Lastochkin D, Wang SC, Chang HC. 2004. Maxwell-Wagner 분극 및 모세관 공명에 의한 새로운 AC 전기 분무 메커니즘. Phys Rev Lett 92:133902.
- ↑ Yeo LY, Gagnon Z, Chang HC. 2005. AC 전기분무 생체재료 합성. 생체재료 26:6122-6218.
- ↑다음으로 이동:9.0 9.1 Wilm M, Mann M. 1996. 나노전기분무 이온 소스의 분석적 특성. Anal Chem 68:1-8.
- ↑ Gabelica V, De Pauw E. 2003. 전기분무 소스에서 생성된 이온의 내부 에너지 및 단편화. Mass Spec Rev 24:566–587.
- ↑ Morozov VN, Morozov TY. 1999. 생물학적 및 생물학적으로 활성인 물질의 단일 및 다중 구성 요소 마이크로어레이의 대량 제작을 위한 방법으로서의 전기분무 증착. Anal Chem 71:3110-3117.
- ↑ Okubo Y, Ikemoto K, Koike K, Tsutsui C, Sakata I, Takei O, Adachi A, Sakai T. 2008. 전기분무 공정을 통한 물방울 충격에 의한 살아있는 세포로의 DNA 도입. Angew Chem Int Ed 47:1429-1431.
- ↑ Leu TS, Teng CH. 2006. 마이크로 전기분무 칩의 설계, 제작 및 연구. Mater Sci Forum 505-507:1249-1254.
- ↑ Jaworek A. 2007. 박막 증착을 위한 전기 분무 물방울 소스. J Mater Sci 42:266–297.